
近日,北京大学药学院天然药物及仿生药物全国重点实验室曾克武与屠鹏飞团队在国际学术期刊ACS Nano上发表了题为“In Situ Redox-Omics Decoding of Nanoparticle-Protein Corona Interactions Drives the Mitochondrial Metabolic-Immunological Mechanism in Microglia”的研究论文,深入揭示了中药野马追(Eupatorium lindleyanum, EL) 所形成的碳量子点通过调控蛋白的氧化/还原“开关”发挥抗脑缺血损伤的全新分子机制。

中药材在炮制、煎煮到制剂的过程中普遍存在不同纳米形态的产物,这主要源于中药里的糖类、黄酮、生物碱等多种活性成分,它们能够通过自组装形成独特的纳米结构,这一特性有助于提高药物溶解度并增强药理活性。本研究首次以中药材野马追为碳源制备出碳量子点,随后采用氧化还原蛋白质组学策略鉴定出其互作靶点,最终阐明其抗脑缺血的分子机制。该研究突破了传统天然产物研究在单分子尺度上的局限,将探索视角拓展至纳米尺度,为解析中药复杂体系的作用机制开辟了新的维度。
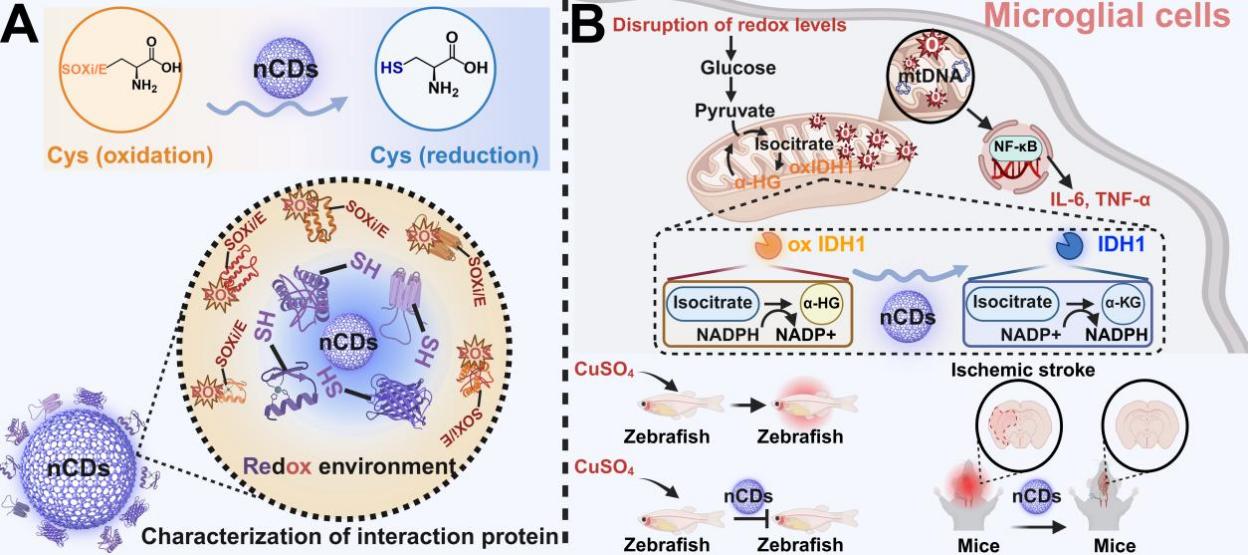
曾克武与屠鹏飞团队首先以野马追为碳源,采用溶剂热的方法成功制备出碳量子点,随后采用氧化还原蛋白质组学策略鉴别出IDH1为其关键的结合蛋白。进一步研究发现,碳量子点通过选择性逆转IDH1的NADP+识别结构域的构象恢复IDH1的酶活性,进而维持线粒体的完整性并抑制mtDNA-cGAS-STING信号通路的激活,最终在斑马鱼的OGD/R模型及小鼠的MCAO模型上证实了碳量子点具有抗脑缺血损伤的作用。该研究不仅揭示了中药碳量子点通过调控IDH1的氧化/还原态发挥抗脑缺血损伤的分子机制,也为脑缺血损伤的治疗提供了新的潜在靶点。
该研究的第一完成单位是北京大学药学院天然药物及仿生药物全国重点实验室,北京大学药学院曾克武教授、屠鹏飞教授为本文的共同通讯作者,北京大学药学院2023级硕士生陈泽坤,博士后余明(现工作于遵义医科大学)为共同第一作者。该工作获得了国家自然科学基金等项目的资助。
论文链接:https://doi.org/10.1021/acsnano.5c21740
通讯作者简介:

曾克武,教授,博士生导师,国家杰出青年基金获得者、青年长江学者、青年岐黄学者。长期从事天然活性分子探针的发现与药物靶标鉴定研究,以通讯作者在PNAS,Sci Adv,ACS Cent Sci,ACS Nano,Adv Sci等国际学术期刊发表系列研究论文130余篇,研究成果入选2017年度“中国十大医学进展”、2022年度“中医药十大学术进展”及2024/2025年度国际中医药与传统医药高影响力研究,申请发明专利11项,承担基金委、科技部、国际合作等科研课题12项,目前担任世界中医药学会联合会、中国中西医结合学会、中国药理学会等学术团体的理事、委员和青年委员等职务。

屠鹏飞,教授,博士生导师,国家杰出青年基金获得者、首批岐黄学者、国家药典委员会执委。承担了国家和省部级项目70余项,成功创制有效部位新药2项,获得新药证书4个。以通讯作者在PNAS、Nat Commun等国际知名期刊发表论文400余篇,著作19部,授权专利169件。研究成果以第一完成人获得国家科技进步奖二等奖2项,教育部等部级科技成果奖一等奖5项,并获得2016年度“全国脱贫攻坚奖”和“最美生态公益人物”、2017年度“全国创新争先奖奖状”和“吴阶平医药创新奖”、第十六届中国药学发展奖创新药物特别贡献奖、第三批“全国高校黄大年式教师团队”带头人等荣誉。
天然药物及仿生药物全国重点实验室
北京大学中医药现代研究中心 供稿