
2026年2月8日,我院天然药物及仿生药物全国重点实验室汤新景和杨振军研究团队在学术期刊Journal of Medicinal Chemistry上发表了最新研究成果“Targeted Degradation of Lin28B Using Pre-let-7-PROTACs for Hepatocellular Carcinoma Therapy”。

目前,中国肝癌的新发患者占世界肝癌42%以上, 是中国高发且致死率极高的恶性肿瘤之一,尤其是肝细胞癌(HCC)。目前临床治疗手段有限,术后转移和复发率高,急需发展新型靶向治疗策略。Lin28B是一种肿瘤干性因子,是多种肿瘤中高表达的RNA结合蛋白。它通过特异性结合miRNA let-7前体(pri-let-7或pre-let-7)从而抑制具有抑癌作用的let-7家族miRNA的成熟过程,促进肿瘤干细胞特性的维持,参与肿瘤的耐药、转移和复发过程。然而,由于Lin28B蛋白表面缺乏传统小分子结合口袋,长期以来被视为“不可成药”靶点。
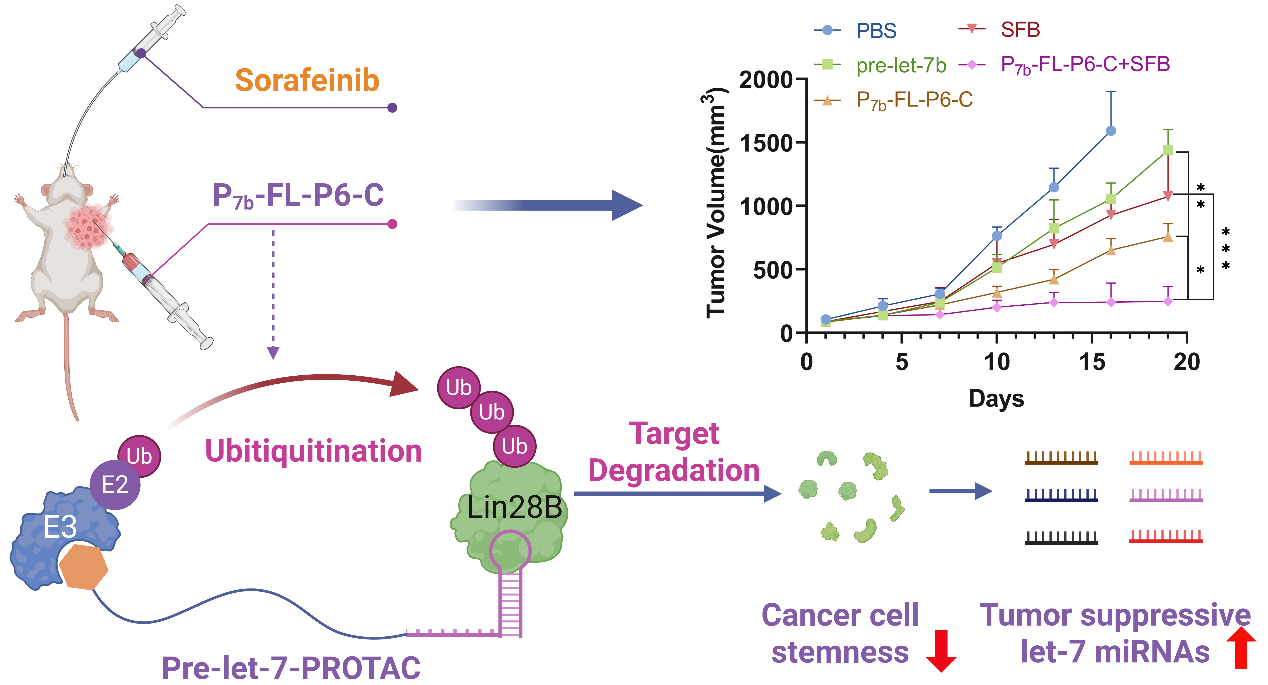
汤新景团队创新性地利用pre-let-7作为靶向配体,在前期pre-let-7f-PROTAC的研究工作基础上(Science Advances,2024),通过不同长度和类型的连接臂将不同pre-let-7序列与E3泛素连接酶配体(泊马度胺或VH032)偶联,构建了一系列基于pre-let-7家族序列的PROTAC嵌合核酸分子库(pre-let-7-PROTACs),pre-let-7负责识别并结合Lin28B,E3配体则招募泛素连接酶系统,从而引导Lin28B通过泛素-蛋白酶体途径被降解。
研究团队系统筛选并优选出了高效降解Lin28B的最优PROTAC分子 P7b-FL-P6-C。该分子在低浓度和短时间内即可将Huh-7肝癌细胞中的Lin28B蛋白水平降至约10%,并显著恢复内源性成熟let-7 miRNA的表达。进一步功能实验表明,P7b-FL-P6-C可有效抑制肝癌细胞增殖与迁移,促进细胞凋亡,并增强对临床使用的肝癌化疗药物索拉非尼的敏感性。在Huh-7移植瘤小鼠模型中,P7b-FL-P6-C单独治疗显著抑制肿瘤生长,肿瘤体积和重量分别下降约50%。更重要的是,其与索拉非尼联用表现出强协同抗肿瘤效果,肿瘤抑制率达到70%-80%,且未引起明显系统毒性。
该研究将miRNA let-7 前体(pre-let-7)应用于PROTAC设计,成功实现了对“不可成药”靶点Lin28B的靶向降解,为肝癌治疗提供了全新的策略和候选分子。该工作不仅拓展了核酸PROTAC的应用范围,也为基于miRNA的肿瘤治疗开辟了新的研究方向。
北京大学药学院博士后许建飞与2023级博士研究生梁星星为该论文的第一共同作者,北京大学药学院汤新景教授为该论文的通讯作者。
论文链接:https://pubs.acs.org/doi/full/10.1021/acs.jmedchem.5c03203
第一作者简介:

许建飞,北京大学药学院博士后,研究方向为核酸药物化学。目前以第一作者(含共同第一作者)在Sci. Adv.、J. Med. Chem.等期刊上发表7篇学术论文。主持中国博士后科学基金第78批面上项目一项。

梁星星,北京大学药学院2023级博士研究生,研究方向为核酸药物化学。目前以第一作者或者共同作者在J. Med. Chem.、Sci. Adv.等期刊上发表多篇学术论文。在读期间获得“北京大学优秀科研奖”等荣誉。
天然药物及仿生药物全国重点实验室 供稿